ಪಿಸಿಆರ್ ಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ, ಕೆಲವು ಮಧ್ಯಪ್ರವೇಶಿಸುವ ಅಂಶಗಳು ಹೆಚ್ಚಾಗಿ ಎದುರಾಗುತ್ತವೆ.
PCR ನ ಅತಿ ಹೆಚ್ಚಿನ ಸಂವೇದನೆಯಿಂದಾಗಿ, ಮಾಲಿನ್ಯವು PCR ಫಲಿತಾಂಶಗಳ ಮೇಲೆ ಪರಿಣಾಮ ಬೀರುವ ಪ್ರಮುಖ ಅಂಶಗಳಲ್ಲಿ ಒಂದಾಗಿದೆ ಎಂದು ಪರಿಗಣಿಸಲಾಗಿದೆ ಮತ್ತು ಇದು ತಪ್ಪು ಸಕಾರಾತ್ಮಕ ಫಲಿತಾಂಶಗಳನ್ನು ಉಂಟುಮಾಡಬಹುದು.
ತಪ್ಪು-ಋಣಾತ್ಮಕ ಫಲಿತಾಂಶಗಳಿಗೆ ಕಾರಣವಾಗುವ ವಿವಿಧ ಮೂಲಗಳು ಅಷ್ಟೇ ಮುಖ್ಯ. ಪಿಸಿಆರ್ ಮಿಶ್ರಣದ ಒಂದು ಅಥವಾ ಹೆಚ್ಚಿನ ಅಗತ್ಯ ಭಾಗಗಳು ಅಥವಾ ವರ್ಧನೆಯ ಕ್ರಿಯೆಯು ಪ್ರತಿಬಂಧಿಸಲ್ಪಟ್ಟರೆ ಅಥವಾ ಹಸ್ತಕ್ಷೇಪ ಮಾಡಿದರೆ, ರೋಗನಿರ್ಣಯದ ವಿಶ್ಲೇಷಣೆಗೆ ಅಡ್ಡಿಯಾಗಬಹುದು. ಇದು ಕಡಿಮೆ ದಕ್ಷತೆ ಮತ್ತು ತಪ್ಪು-ಋಣಾತ್ಮಕ ಫಲಿತಾಂಶಗಳಿಗೆ ಕಾರಣವಾಗಬಹುದು.
ಪ್ರತಿಬಂಧದ ಜೊತೆಗೆ, ಮಾದರಿ ತಯಾರಿಕೆಗೆ ಮುಂಚಿತವಾಗಿ ಸಾಗಣೆ ಮತ್ತು/ಅಥವಾ ಶೇಖರಣಾ ಪರಿಸ್ಥಿತಿಗಳಿಂದಾಗಿ ಗುರಿ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲದ ಸಮಗ್ರತೆಯ ನಷ್ಟ ಸಂಭವಿಸಬಹುದು. ನಿರ್ದಿಷ್ಟವಾಗಿ ಹೇಳುವುದಾದರೆ, ಹೆಚ್ಚಿನ ತಾಪಮಾನ ಅಥವಾ ಅಸಮರ್ಪಕ ಸಂಗ್ರಹಣೆಯು ಜೀವಕೋಶಗಳು ಮತ್ತು ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳ ಹಾನಿಗೆ ಕಾರಣವಾಗಬಹುದು. ಕೋಶ ಮತ್ತು ಅಂಗಾಂಶ ಸ್ಥಿರೀಕರಣ ಮತ್ತು ಪ್ಯಾರಾಫಿನ್ ಎಂಬೆಡಿಂಗ್ ಡಿಎನ್ಎ ವಿಘಟನೆ ಮತ್ತು ನಿರಂತರ ಸಮಸ್ಯೆಗೆ ಪ್ರಸಿದ್ಧ ಕಾರಣಗಳಾಗಿವೆ (ಚಿತ್ರಗಳು 1 ಮತ್ತು 2 ನೋಡಿ). ಈ ಸಂದರ್ಭಗಳಲ್ಲಿ, ಸೂಕ್ತವಾದ ಪ್ರತ್ಯೇಕತೆ ಮತ್ತು ಶುದ್ಧೀಕರಣವು ಸಹ ಸಹಾಯ ಮಾಡುವುದಿಲ್ಲ.
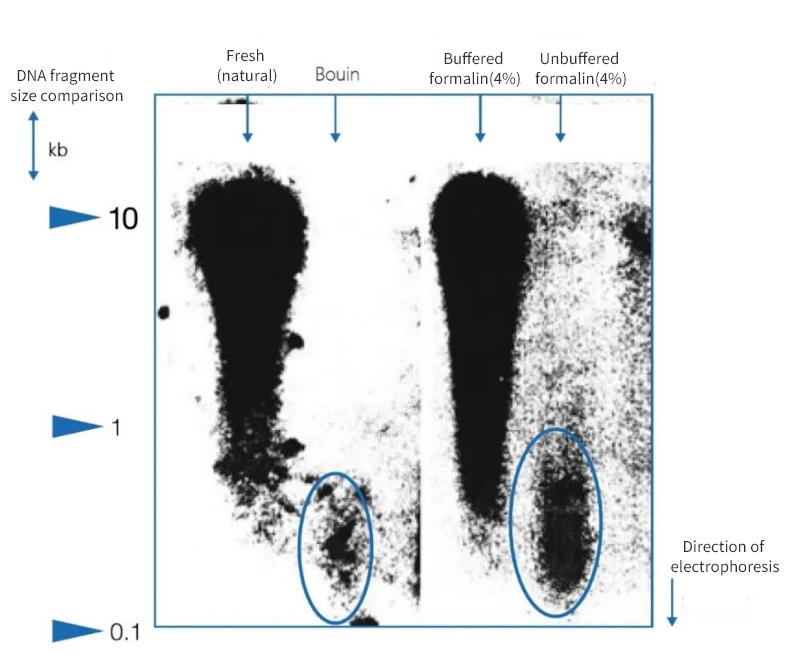
ಚಿತ್ರ 1 | ಡಿಎನ್ಎ ಸಮಗ್ರತೆಯ ಮೇಲೆ ನಿಶ್ಚಲತೆಯ ಪರಿಣಾಮ
ಶವಪರೀಕ್ಷೆಯ ಪ್ಯಾರಾಫಿನ್ ವಿಭಾಗಗಳಿಂದ ಪ್ರತ್ಯೇಕಿಸಲಾದ ಡಿಎನ್ಎಯ ಗುಣಮಟ್ಟ ಗಣನೀಯವಾಗಿ ಬದಲಾಗುತ್ತದೆ ಎಂದು ಅಗರೋಸ್ ಜೆಲ್ ಎಲೆಕ್ಟ್ರೋಫೋರೆಸಿಸ್ ತೋರಿಸಿದೆ. ಸ್ಥಿರೀಕರಣ ವಿಧಾನವನ್ನು ಅವಲಂಬಿಸಿ ಸಾರಗಳಲ್ಲಿ ವಿಭಿನ್ನ ಸರಾಸರಿ ತುಣುಕು ಉದ್ದದ ಡಿಎನ್ಎ ಇತ್ತು. ಸ್ಥಳೀಯ ಹೆಪ್ಪುಗಟ್ಟಿದ ಮಾದರಿಗಳಲ್ಲಿ ಮತ್ತು ಬಫರ್ ಮಾಡಿದ ತಟಸ್ಥ ಫಾರ್ಮಾಲಿನ್ನಲ್ಲಿ ಸ್ಥಿರಗೊಳಿಸಿದಾಗ ಮಾತ್ರ ಡಿಎನ್ಎ ಸಂರಕ್ಷಿಸಲ್ಪಟ್ಟಿತು. ಬಲವಾಗಿ ಆಮ್ಲೀಯ ಬೌಯಿನ್ ಸ್ಥಿರೀಕರಣ ಅಥವಾ ಬಫರ್ ಮಾಡದ, ಫಾರ್ಮಿಕ್ ಆಮ್ಲ-ಒಳಗೊಂಡಿರುವ ಫಾರ್ಮಾಲಿನ್ ಬಳಕೆಯು ಡಿಎನ್ಎಯ ಗಮನಾರ್ಹ ನಷ್ಟಕ್ಕೆ ಕಾರಣವಾಯಿತು. ಉಳಿದ ಭಾಗವು ಹೆಚ್ಚು ಛಿದ್ರಗೊಂಡಿದೆ.
ಎಡಭಾಗದಲ್ಲಿ, ತುಣುಕುಗಳ ಉದ್ದವನ್ನು ಕಿಲೋಬೇಸ್ ಜೋಡಿಗಳಲ್ಲಿ (kbp) ವ್ಯಕ್ತಪಡಿಸಲಾಗಿದೆ.
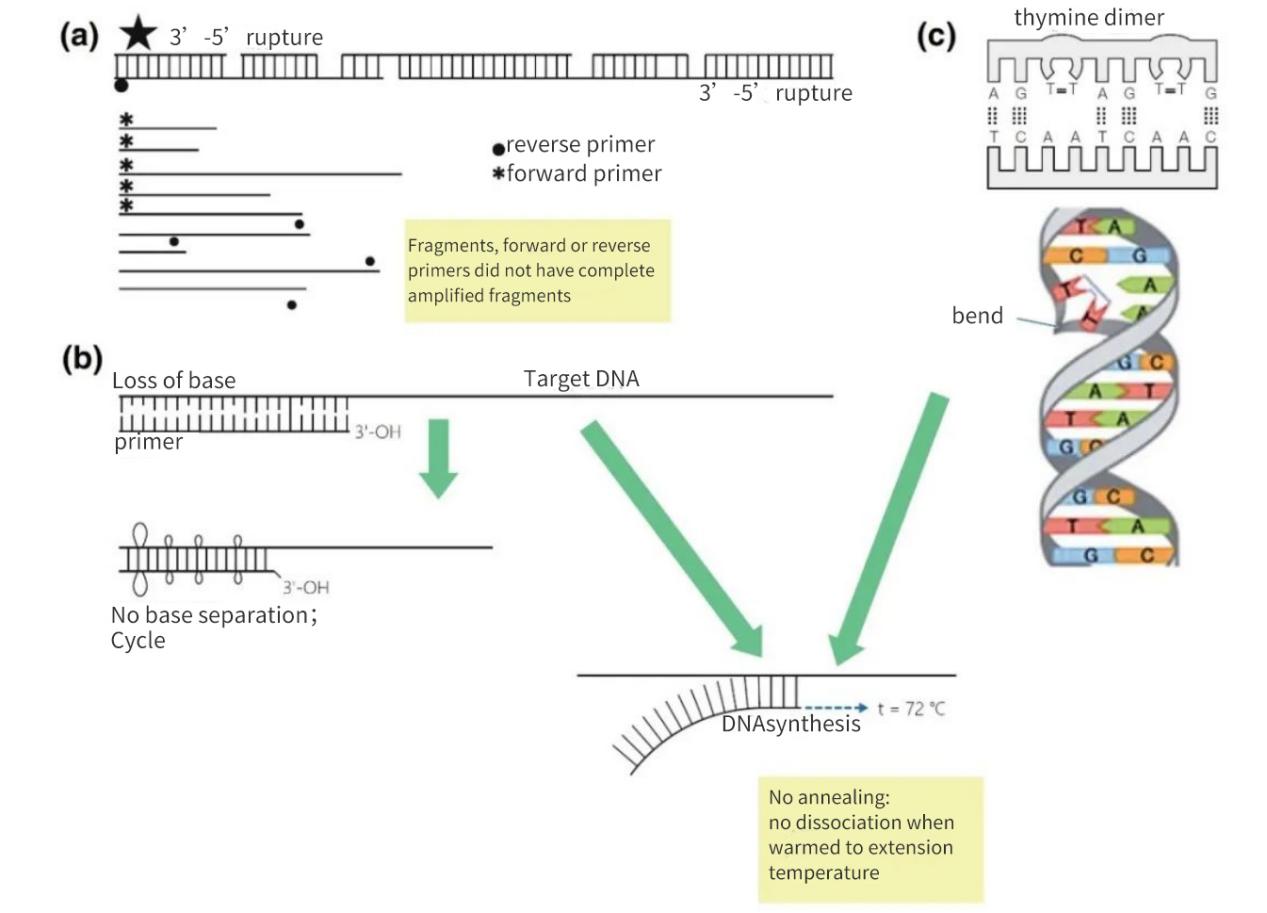
ಚಿತ್ರ 2 | ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲ ಗುರಿಗಳ ಸಮಗ್ರತೆಯ ನಷ್ಟ
(ಎ) ಎರಡೂ ಎಳೆಗಳ ಮೇಲೆ 3′-5′ ಅಂತರವಿದ್ದರೆ ಗುರಿ ಡಿಎನ್ಎಯಲ್ಲಿ ವಿರಾಮ ಉಂಟಾಗುತ್ತದೆ. ಡಿಎನ್ಎ ಸಂಶ್ಲೇಷಣೆ ಇನ್ನೂ ಸಣ್ಣ ತುಣುಕಿನ ಮೇಲೆ ಸಂಭವಿಸುತ್ತದೆ. ಆದಾಗ್ಯೂ, ಡಿಎನ್ಎ ತುಣುಕಿನ ಮೇಲೆ ಪ್ರೈಮರ್ ಅನೆಲಿಂಗ್ ಸೈಟ್ ಕಾಣೆಯಾಗಿದ್ದರೆ, ರೇಖೀಯ ವರ್ಧನೆ ಮಾತ್ರ ಸಂಭವಿಸುತ್ತದೆ. ಅತ್ಯಂತ ಅನುಕೂಲಕರ ಸಂದರ್ಭದಲ್ಲಿ, ತುಣುಕುಗಳು ಪರಸ್ಪರ ಮರುಸಂಗ್ರಹಿಸಬಹುದು, ಆದರೆ ಇಳುವರಿ ಚಿಕ್ಕದಾಗಿರುತ್ತದೆ ಮತ್ತು ಪತ್ತೆ ಮಟ್ಟಕ್ಕಿಂತ ಕಡಿಮೆ ಇರುತ್ತದೆ.
(b) ಮುಖ್ಯವಾಗಿ ಡಿಪ್ಯೂರಿನೇಷನ್ ಮತ್ತು ಥೈಮಿಡಿನ್ ಡೈಮರ್ ರಚನೆಯಿಂದಾಗಿ ಬೇಸ್ಗಳ ನಷ್ಟವು H-ಬಂಧಗಳ ಸಂಖ್ಯೆಯಲ್ಲಿ ಇಳಿಕೆಗೆ ಮತ್ತು Tm ನಲ್ಲಿ ಇಳಿಕೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ. ಉದ್ದವಾದ ತಾಪಮಾನ ಏರಿಕೆಯ ಹಂತದಲ್ಲಿ, ಪ್ರೈಮರ್ಗಳು ಮ್ಯಾಟ್ರಿಕ್ಸ್ DNA ಯಿಂದ ಕರಗುತ್ತವೆ ಮತ್ತು ಕಡಿಮೆ ಕಠಿಣ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿಯೂ ಸಹ ಅನೀಲ್ ಆಗುವುದಿಲ್ಲ.
(ಸಿ) ಪಕ್ಕದ ಥೈಮಿನ್ ಬೇಸ್ಗಳು ಟಿಟಿ ಡೈಮರ್ ಅನ್ನು ರೂಪಿಸುತ್ತವೆ.
ಆಣ್ವಿಕ ರೋಗನಿರ್ಣಯದಲ್ಲಿ ಸಾಮಾನ್ಯವಾಗಿ ಕಂಡುಬರುವ ಮತ್ತೊಂದು ಸಾಮಾನ್ಯ ಸಮಸ್ಯೆಯೆಂದರೆ ಫೀನಾಲ್-ಕ್ಲೋರೋಫಾರ್ಮ್ ಹೊರತೆಗೆಯುವಿಕೆಗೆ ಹೋಲಿಸಿದರೆ ಗುರಿ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳ ಬಿಡುಗಡೆ ಕಡಿಮೆ. ವಿಪರೀತ ಸಂದರ್ಭಗಳಲ್ಲಿ, ಇದು ತಪ್ಪು ನಕಾರಾತ್ಮಕತೆಗಳೊಂದಿಗೆ ಸಂಬಂಧ ಹೊಂದಿರಬಹುದು. ಕುದಿಯುವ ಲೈಸಿಸ್ ಅಥವಾ ಜೀವಕೋಶದ ಶಿಲಾಖಂಡರಾಶಿಗಳ ಕಿಣ್ವಕ ಜೀರ್ಣಕ್ರಿಯೆಯಿಂದ ಹೆಚ್ಚಿನ ಸಮಯವನ್ನು ಉಳಿಸಬಹುದು, ಆದರೆ ಈ ವಿಧಾನವು ಸಾಕಷ್ಟು ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲ ಬಿಡುಗಡೆಯಿಂದಾಗಿ ಕಡಿಮೆ ಪಿಸಿಆರ್ ಸಂವೇದನೆಗೆ ಕಾರಣವಾಗುತ್ತದೆ.
ವರ್ಧನೆಯ ಸಮಯದಲ್ಲಿ ಪಾಲಿಮರೇಸ್ ಚಟುವಟಿಕೆಯ ಪ್ರತಿಬಂಧ
ಸಾಮಾನ್ಯವಾಗಿ, ಸಬ್ಆಪ್ಟಿಮಲ್ ಪಿಸಿಆರ್ ಫಲಿತಾಂಶಗಳಿಗೆ ಕಾರಣವಾಗುವ ಎಲ್ಲಾ ಅಂಶಗಳನ್ನು ವಿವರಿಸಲು ಪ್ರತಿಬಂಧವನ್ನು ಧಾರಕ ಪರಿಕಲ್ಪನೆಯಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಕಟ್ಟುನಿಟ್ಟಾಗಿ ಜೀವರಾಸಾಯನಿಕ ಅರ್ಥದಲ್ಲಿ, ಪ್ರತಿಬಂಧವು ಕಿಣ್ವದ ಚಟುವಟಿಕೆಗೆ ಸೀಮಿತವಾಗಿದೆ, ಅಂದರೆ, ಇದು ಡಿಎನ್ಎ ಪಾಲಿಮರೇಸ್ನ ಸಕ್ರಿಯ ಸೈಟ್ ಅಥವಾ ಅದರ ಕೊಫ್ಯಾಕ್ಟರ್ನೊಂದಿಗೆ (ಉದಾ., ಟಕ್ ಡಿಎನ್ಎ ಪಾಲಿಮರೇಸ್ಗಾಗಿ ಎಂಜಿ2+) ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಮೂಲಕ ತಲಾಧಾರ-ಉತ್ಪನ್ನ ಪರಿವರ್ತನೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುತ್ತದೆ ಅಥವಾ ತಡೆಯುತ್ತದೆ.
ಮಾದರಿಯಲ್ಲಿರುವ ಘಟಕಗಳು ಅಥವಾ ಕಾರಕಗಳನ್ನು ಹೊಂದಿರುವ ವಿವಿಧ ಬಫರ್ಗಳು ಮತ್ತು ಸಾರಗಳು ನೇರವಾಗಿ ಕಿಣ್ವವನ್ನು ಪ್ರತಿಬಂಧಿಸಬಹುದು ಅಥವಾ ಅದರ ಸಹ-ಅಂಶಕಗಳನ್ನು (ಉದಾ. EDTA) ಬಲೆಗೆ ಬೀಳಿಸಬಹುದು, ಇದರಿಂದಾಗಿ ಪಾಲಿಮರೇಸ್ ಅನ್ನು ನಿಷ್ಕ್ರಿಯಗೊಳಿಸಬಹುದು ಮತ್ತು ಪ್ರತಿಯಾಗಿ ಕಡಿಮೆ ಅಥವಾ ತಪ್ಪು-ಋಣಾತ್ಮಕ PCR ಫಲಿತಾಂಶಗಳಿಗೆ ಕಾರಣವಾಗಬಹುದು.
ಆದಾಗ್ಯೂ, ಪ್ರತಿಕ್ರಿಯಾ ಘಟಕಗಳು ಮತ್ತು ಗುರಿ-ಒಳಗೊಂಡಿರುವ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳ ನಡುವಿನ ಅನೇಕ ಪರಸ್ಪರ ಕ್ರಿಯೆಗಳನ್ನು 'PCR ಪ್ರತಿರೋಧಕಗಳು' ಎಂದು ಸಹ ಗೊತ್ತುಪಡಿಸಲಾಗುತ್ತದೆ. ಪ್ರತ್ಯೇಕತೆಯಿಂದ ಜೀವಕೋಶದ ಸಮಗ್ರತೆಯು ಅಡ್ಡಿಪಡಿಸಲ್ಪಟ್ಟ ನಂತರ ಮತ್ತು ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲ ಬಿಡುಗಡೆಯಾದ ನಂತರ, ಮಾದರಿ ಮತ್ತು ಅದರ ಸುತ್ತಮುತ್ತಲಿನ ದ್ರಾವಣ ಮತ್ತು ಘನ ಹಂತದ ನಡುವಿನ ಪರಸ್ಪರ ಕ್ರಿಯೆಗಳು ಸಂಭವಿಸಬಹುದು. ಉದಾಹರಣೆಗೆ, 'ಸ್ಕ್ಯಾವೆಂಜರ್ಗಳು' ಕೋವೆಲನ್ಸಿಯಲ್ಲದ ಪರಸ್ಪರ ಕ್ರಿಯೆಗಳ ಮೂಲಕ ಏಕ ಅಥವಾ ಡಬಲ್-ಸ್ಟ್ರಾಂಡೆಡ್ DNA ಯನ್ನು ಬಂಧಿಸಬಹುದು ಮತ್ತು ಅಂತಿಮವಾಗಿ PCR ಪ್ರತಿಕ್ರಿಯಾ ಪಾತ್ರೆಯನ್ನು ತಲುಪುವ ಗುರಿಗಳ ಸಂಖ್ಯೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುವ ಮೂಲಕ ಪ್ರತ್ಯೇಕತೆ ಮತ್ತು ಶುದ್ಧೀಕರಣಕ್ಕೆ ಅಡ್ಡಿಪಡಿಸಬಹುದು.
ಸಾಮಾನ್ಯವಾಗಿ, ಪಿಸಿಆರ್ ಪ್ರತಿರೋಧಕಗಳು ಹೆಚ್ಚಿನ ದೇಹದ ದ್ರವಗಳು ಮತ್ತು ಕ್ಲಿನಿಕಲ್ ರೋಗನಿರ್ಣಯ ಪರೀಕ್ಷೆಗಳಿಗೆ ಬಳಸುವ ಕಾರಕಗಳಲ್ಲಿ (ಮೂತ್ರದಲ್ಲಿ ಯೂರಿಯಾ, ರಕ್ತದಲ್ಲಿ ಹಿಮೋಗ್ಲೋಬಿನ್ ಮತ್ತು ಹೆಪಾರಿನ್), ಆಹಾರ ಪೂರಕಗಳು (ಸಾವಯವ ಘಟಕಗಳು, ಗ್ಲೈಕೋಜನ್, ಕೊಬ್ಬು, Ca2+ ಅಯಾನುಗಳು) ಮತ್ತು ಪರಿಸರದಲ್ಲಿನ ಘಟಕಗಳಲ್ಲಿ (ಫೀನಾಲ್ಗಳು, ಭಾರ ಲೋಹಗಳು) ಇರುತ್ತವೆ.
| ಪ್ರತಿರೋಧಕಗಳು | ಮೂಲ |
| ಕ್ಯಾಲ್ಸಿಯಂ ಅಯಾನುಗಳು | ಹಾಲು, ಮೂಳೆ ಅಂಗಾಂಶ |
| ಕಾಲಜನ್ | ಅಂಗಾಂಶ |
| ಪಿತ್ತರಸ ಲವಣಗಳು | ಮಲ |
| ಹಿಮೋಗ್ಲೋಬಿನ್ | ರಕ್ತದಲ್ಲಿ |
| ಹಿಮೋಗ್ಲೋಬಿನ್ | ರಕ್ತದ ಮಾದರಿಗಳು |
| ಹ್ಯೂಮಿಕ್ ಆಮ್ಲ | ಮಣ್ಣು, ಸಸ್ಯ |
| ರಕ್ತ | ರಕ್ತ |
| ಲ್ಯಾಕ್ಟೋಫೆರಿನ್ | ರಕ್ತ |
| (ಯುರೋಪಿಯನ್) ಮೆಲನಿನ್ | ಚರ್ಮ, ಕೂದಲು |
| ಮಯೋಗ್ಲೋಬಿನ್ | ಸ್ನಾಯು ಅಂಗಾಂಶ |
| ಪಾಲಿಸ್ಯಾಕರೈಡ್ಗಳು | ಸಸ್ಯ, ಮಲ |
| ಪ್ರೋಟೀಸ್ | ಹಾಲು |
| ಯೂರಿಯಾ | ಮೂತ್ರ |
| ಮ್ಯೂಕೋಪಾಲಿಸ್ಯಾಕರೈಡ್ | ಕಾರ್ಟಿಲೆಜ್, ಲೋಳೆಯ ಪೊರೆಗಳು |
| ಲಿಗ್ನಿನ್, ಸೆಲ್ಯುಲೋಸ್ | ಸಸ್ಯಗಳು |
ಹೆಚ್ಚು ಪ್ರಚಲಿತ ಪಿಸಿಆರ್ ಪ್ರತಿರೋಧಕಗಳು ಬ್ಯಾಕ್ಟೀರಿಯಾ ಮತ್ತು ಯುಕ್ಯಾರಿಯೋಟಿಕ್ ಕೋಶಗಳು, ಗುರಿಯಿಲ್ಲದ ಡಿಎನ್ಎ, ಅಂಗಾಂಶ ಮ್ಯಾಟ್ರಿಕ್ಸ್ಗಳ ಡಿಎನ್ಎ-ಬಂಧಿಸುವ ಮ್ಯಾಕ್ರೋಮಾಲಿಕ್ಯೂಲ್ಗಳು ಮತ್ತು ಕೈಗವಸುಗಳು ಮತ್ತು ಪ್ಲಾಸ್ಟಿಕ್ಗಳಂತಹ ಪ್ರಯೋಗಾಲಯ ಉಪಕರಣಗಳಲ್ಲಿ ಕಂಡುಬರುತ್ತವೆ. ಪಿಸಿಆರ್ ಪ್ರತಿರೋಧಕಗಳನ್ನು ಹೊರತೆಗೆಯುವ ಸಮಯದಲ್ಲಿ ಅಥವಾ ನಂತರ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳ ಶುದ್ಧೀಕರಣವು ಆದ್ಯತೆಯ ವಿಧಾನವಾಗಿದೆ.
ಇಂದು, ವಿವಿಧ ಸ್ವಯಂಚಾಲಿತ ಹೊರತೆಗೆಯುವ ಉಪಕರಣಗಳು ಅನೇಕ ಹಸ್ತಚಾಲಿತ ಪ್ರೋಟೋಕಾಲ್ಗಳನ್ನು ಬದಲಾಯಿಸಬಹುದು, ಆದರೆ 100% ಚೇತರಿಕೆ ಮತ್ತು/ಅಥವಾ ಗುರಿಗಳ ಶುದ್ಧೀಕರಣವನ್ನು ಎಂದಿಗೂ ಸಾಧಿಸಲಾಗಿಲ್ಲ. ಶುದ್ಧೀಕರಿಸಿದ ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲಗಳಲ್ಲಿ ಸಂಭಾವ್ಯ ಪ್ರತಿರೋಧಕಗಳು ಇನ್ನೂ ಇರಬಹುದು ಅಥವಾ ಈಗಾಗಲೇ ಪರಿಣಾಮ ಬೀರಿರಬಹುದು. ಪ್ರತಿರೋಧಕಗಳ ಪರಿಣಾಮವನ್ನು ಕಡಿಮೆ ಮಾಡಲು ವಿಭಿನ್ನ ತಂತ್ರಗಳು ಅಸ್ತಿತ್ವದಲ್ಲಿವೆ. ಸೂಕ್ತವಾದ ಪಾಲಿಮರೇಸ್ನ ಆಯ್ಕೆಯು ಪ್ರತಿರೋಧಕ ಚಟುವಟಿಕೆಯ ಮೇಲೆ ಗಮನಾರ್ಹ ಪರಿಣಾಮ ಬೀರುತ್ತದೆ. PCR ಪ್ರತಿಬಂಧವನ್ನು ಕಡಿಮೆ ಮಾಡಲು ಇತರ ಸಾಬೀತಾದ ವಿಧಾನಗಳು ಪಾಲಿಮರೇಸ್ ಸಾಂದ್ರತೆಯನ್ನು ಹೆಚ್ಚಿಸುವುದು ಅಥವಾ BSA ನಂತಹ ಸೇರ್ಪಡೆಗಳನ್ನು ಅನ್ವಯಿಸುವುದು.
ಆಂತರಿಕ ಪ್ರಕ್ರಿಯೆ ಗುಣಮಟ್ಟ ನಿಯಂತ್ರಣ (ಐಪಿಸಿ) ಬಳಕೆಯಿಂದ ಪಿಸಿಆರ್ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಪ್ರತಿಬಂಧವನ್ನು ಪ್ರದರ್ಶಿಸಬಹುದು.
ಹೊರತೆಗೆಯುವ ಕಿಟ್ನಲ್ಲಿರುವ ಎಲ್ಲಾ ಕಾರಕಗಳು ಮತ್ತು ಇತರ ದ್ರಾವಣಗಳಾದ ಎಥೆನಾಲ್, EDTA, CETAB, LiCl, GuSCN, SDS, ಐಸೊಪ್ರೊಪನಾಲ್ ಮತ್ತು ಫೀನಾಲ್ಗಳನ್ನು ನ್ಯೂಕ್ಲಿಯಿಕ್ ಆಮ್ಲ ಐಸೋಲೇಟ್ನಿಂದ ಸಂಪೂರ್ಣ ತೊಳೆಯುವ ಹಂತದ ಮೂಲಕ ತೆಗೆದುಹಾಕಲು ಕಾಳಜಿ ವಹಿಸಬೇಕು. ಅವುಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಅವಲಂಬಿಸಿ, ಅವು PCR ಅನ್ನು ಸಕ್ರಿಯಗೊಳಿಸಬಹುದು ಅಥವಾ ಪ್ರತಿಬಂಧಿಸಬಹುದು.
ಪೋಸ್ಟ್ ಸಮಯ: ಮೇ-19-2023
 中文网站
中文网站